A case of clozapine-induced myoclonic epilepsy
Clozapine is effective in treatment-resistant schizophrenia. However, clozapine has its own (well-) known side effects. We describe a case of a patient who developed epileptic seizures after starting clozapine. First he had a tonic-clonic seizure and subsequently myoclonic seizures. It is relevant to recognize the epileptic origin of these events. If tapering the clozapine dosage is not possible, the myoclonic seizures are treatable with anti-epileptic drugs. We describe the case history of this patient, the differential diagnosis and the evidence of a correlation between myoclonic epilepsy and clozapine based on international literature.
Clozapine is een dibenzodiazepinederivaat met antipsychotische werking.1 Het heeft sterke noradrenolytische, parasympathicolytische en antihistaminerge eigenschappen en wordt gebruikt voor de behandeling van therapieresistente schizofrenie die niet, of onvoldoende reageert op ten minste twee andere antipsychotica (waaronder een atypisch middel) of waarbij andere antipsychotica onbehandelbare bijwerkingen geven.1 Bekende bijwerkingen van clozapine zijn onder andere gewichtstoename (bij > 35%),2,3 slaperigheid, duizeligheid, obstipatie, hypersalivatie en tachycardie (> 10% van de gevallen) en urineverlies (1-10%).1 Er wordt geadviseerd om voorzichtig te zijn bij de behandeling van patiënten met epilepsie omdat dosisgerelateerde epileptische aanvallen zijn gemeld.1
Myoklonieën staan niet beschreven als bijwerking van clozapine in het Farmacotherapeutisch kompas of bij het bijwerkingencentrum Lareb, maar staan wel genoemd in de Nederlandse richtlijn voor het gebruik van clozapine en de Glasgow Antipsychotic Side-effects Scale for Clozapine (GASS-C).4,5 Uit de literatuur blijkt dat myoklonieën en tonisch-klonische aanvallen (TC’s) geïnduceerd door clozapine, vaak voorkomen bij patiënten die geen epilepsie in de voorgeschiedenis hebben.6-10 Na een casusbeschrijving van een patiënt met hinderlijke schokken bespreken we aan de hand van internationale wetenschappelijke literatuur het vóórkomen en het belang van herkennen van epileptische myoklonieën.
Casusbeschrijving
Patiënt A, een 48-jarige man, kwam op de polikliniek bij de neuroloog in verband met hinderlijke schokken in de ledematen. Hij had therapieresistente schizofrenie waarvoor hij al 27 jaar clozapine 175 mg per dag gebruikte (startdosering of opbouw onbekend). De dag na het starten van de clozapine had patiënt destijds een tonisch-klonische aanval (TC) gekregen en was men direct gestart met valproïnezuur (opgebouwd tot 2100 mg/dag). De daaropvolgende jaren had hij geen TC’s meer en waren de psychische klachten nagenoeg stabiel gebleven.
Drie jaar voor de huidige episode werd er osteopenie vastgesteld door een internist, geduid als bijwerking van valproïnezuur. De dosering valproïnezuur werd toen verlaagd en patiënt kreeg osteoporoseprofylaxe in de vorm van calciumcarbonaat en colecalciferol. Bij een val twee jaar later brak patiënt zijn rechter scheenbeen. Hij werd opgenomen in het ziekenhuis op de chirurgieafdeling en geopereerd. Valproïnezuur werd verder afgebouwd. Tijdens deze opname kreeg hij een psychotische terugval. De clozapine werd daarop verhoogd naar 300 mg per dag. Patiënt kreeg opnieuw een TC, waarna de valproïnezuur weer in lage dosering werd herstart. Er ontstonden echter schokken in de ledematen en hij zakte frequent door de benen, waarbij hij viel en wederom een fractuur opliep.
Bij het huidige bezoek aan de neuroloog was zijn hulpvraag hoe hij van de hinderlijke schokken af kon komen. Ten tijde van het consult woonde patiënt weer bij zijn ouders en liep hij met rollator, uit angst om opnieuw te vallen.
Er werd een langdurige (video-)elektro-encefalografie(eeg-)registratie verricht om de schokken te classificeren. Ten tijde van de spontaan optredende schokken van de ledematen werden er focale specifiek epileptiforme afwijkingen op het eeg gezien (figuur 1). Hierdoor waren de schokken te classificeren als epileptische myoklonieën. Over de centrale hersengebieden was er tevens een overmaat aan trage activiteit zichtbaar. Laboratoriumonderzoek toonde geen toxische medicatiespiegels (valproïnezuur 74 mg/l en clozapine 0,330 mg/l). Gezien de tijdsrelatie tussen het ontstaan van de myoklonieën en de dosisverhoging van de clozapine, werden deze epileptische myoklonieën geduid als mogelijke bijwerking van clozapine. Valproïnezuur werd verhoogd naar 3000 mg en er werd gestart met topiramaat (2 dd 50 mg). De clozapine werd in overleg met de psychiater verlaagd naar 175 mg; de dosis waar hij eerder jarenlang een stabiel psychiatrisch toestandsbeeld op had.
Figuur 1. Eeg van patiënt ten tijde van de myoklonieën
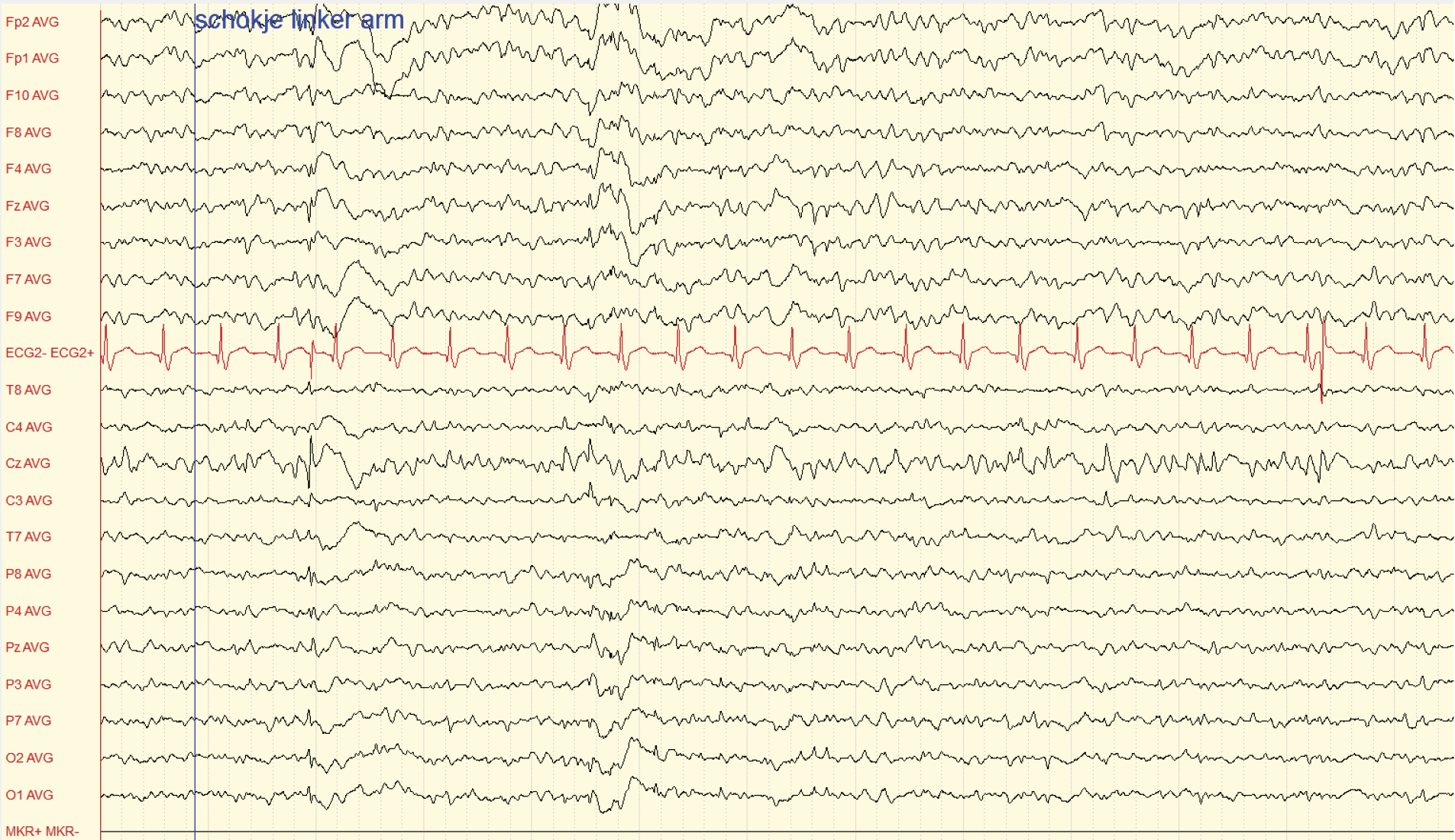
Eeg wordt getoond in de gemiddelde referentieafleiding.* Piekgolfcomplex midcentraal (Cz) exact ten tijde van een schokje in de linkerschouder. Tevens midcentraal continue trage activiteit (afwisselend alfa/thèta/delta-activiteit).
*Van een elektrode wordt het gemiddelde potentiaal van alle elektroden afgetrokken, iedere elektrode wordt ten opzicht van dezelfde referentie bepaald.
Drie weken later volgde een controle-eeg waarop een afname te zien was van de trage activiteit en de specifiek epileptiforme afwijkingen. Op dat moment had patiënt nog 1-2 schokjes per dag, hij viel niet meer en had geen TC’s meer. Zes maanden later traden er in het geheel geen TC’s of myoklonieën meer op.
Bespreking
Myoklonieën
Een myoclonus is een snelle schokbeweging in één of meerdere spiergroepen die ontstaat als gevolg van een neuronale ontlading.11 Myoklonieën kunnen zich (multi)focaal, segmentaal of gegeneraliseerd voordoen. De oorsprong van een myoclonus kan corticaal, subcorticaal of perifeer zijn. Bij een corticale (epileptische) myoclonus kan er tijdens eeg-registratie, 15-40 ms voorafgaande aan de schok, een elektrische ontlading worden gemeten in de vorm van een piekgolfcomplex ter plaatse van de motorische cortex (zoals bij deze casus, zie figuur 1).11
Clozapinegeïnduceerde (corticale/epileptische) myoklonieën
Bij onze patiënt was er een sterk vermoeden dat de eeg-afwijkingen alsmede de epileptische myoklonieën werden veroorzaakt door het gebruik van clozapine. Om deze hypothese te ondersteunen verrichtten we een PubMed-search naar wetenschappelijke studies over het percentage eeg-bewezen corticale myoklonieën ten tijde van behandeling met clozapine (zie online-bijlage). Studies waarbij voor en tijdens het gebruik van clozapine eeg’s zijn verricht, werden geselecteerd en we bespreken deze beknopt in chronologische volgorde. Bij alle vier de studies ontstonden de eeg-afwijkingen en de epileptische myoklonieën pas na het starten van de clozapine, wat pleit voor het veronderstelde oorzakelijke verband.12-15
In de eerste prospectieve studie zijn in 1990 35 patiënten met schizofrenie geïncludeerd uit het New Hampshire Hospital.12 Het eeg voor de start van clozapine was bij allen normaal en werd herhaald bij 300 mg clozapinegebruik, na elke drie maanden en op indicatie. In het beloop kreeg 86% (30/35) een vertraging van het grondpatroon op het eeg. 7 patiënten (20%) kregen één of meerdere epileptische aanvallen; 5 (14%) gegeneraliseerde TC’s, 2 (5%) focale aanvallen en 3 (9%) myoklonische aanvallen.12
De tweede studie betreft een cohortonderzoek waarbij er retrospectief is gekeken naar de eeg’s van patiënten met schizofrenie onder langdurige behandeling met een klassiek antipsychoticum versus clozapine.13 Patiënten die eerder een epileptische aanval hadden doorgemaakt of afwijkingen hadden op eeg of MRI vóór de start van clozapine werden geëxcludeerd. Van de 40 patiënten (25%) kregen er 10 (25%) een afwijkend eeg tijdens clozapinebehandeling. Al deze eeg’s toonden een overmaat aan trage activiteit, bij 7 (18%) patiënten was er sprake van specifiek epileptiforme afwijkingen en in een deel van de gevallen werd daarbij een schokje geobserveerd. Eén patiënt (3%) kreeg een TC. Bij het verlagen van de dosering clozapine en/of starten van valproïnezuur nam het aantal myoklonieën af en werden de eeg-afwijkingen minder uitgesproken.13
In de derde studie beschrijft men eeg-bevindingen bij 26 patiënten met schizofrenie voor en tijdens clozapinegebruik.14 Voor start van de medicatie waren alle eeg’s normaal. Tijdens behandeling werden er bij 10 patiënten (39%) eeg-afwijkingen gevonden; alle 10 hadden specifiek epileptiforme afwijkingen, bij 4 patiënten (15%) werd trage activiteit geconstateerd. Deze patiënten waren gemiddeld jonger en hadden een kortere ziekteduur dan patiënten zonder eeg-afwijkingen. 2 patiënten (8%) kregen een TC en 5 patiënten (19%) myoklonieën. Behandeling met valproïnezuur leidde tot afname van klachten.14
Met de vierde studie wilde men risicofactoren voor afwijkingen van het centrale zenuwstelsel (eeg-afwijkingen, myoclonus of een epileptische aanval) bij clozapine in kaart brengen; het betrof een retrospectief onderzoek onder 106 patiënten met behandelresistente schizofrenie.15 Patiënten met hersenaandoeningen of neurologische complicaties in de voorgeschiedenis werden geëxcludeerd, evenals patiënten met slechte therapietrouw. Eeg’s voor start van de behandeling waren bij de geïncludeerde patiënten normaal. Er werden afwijkingen op het eeg gezien bij 57 patiënten (53,8%), myoklonieën bij 41 patiënten (38,7%) en een TC bij 9 patiënten (8,5%). Patiënten die tegelijkertijd lithium gebruikten (onafhankelijk van de dosis) of die een kortere ziekteduur hadden voor de start van clozapine hadden een grotere kans op één van deze bijwerkingen. Dit gold niet voor de clozapinedosering, -plasmaspiegels of innamefrequentie in deze studie.15
Deze vier studies hebben beperkingen: alle betreffen een analyse vanuit één centrum. Vanwege retrospectieve data-analyse bij twee studies is er een potentiële selectiebias; patiënten die geen eeg voor aanvang van de clozapine hebben gehad zijn geëxcludeerd.13,15 De eeg’s betreffen momentopnames en er werd geen standaardduur van de registraties beschreven. Daarnaast zijn er geen genetische data meegenomen in de baselinegegevens zoals de associatie tussen TC’s en CYP1A2-polymorfisme.16
Belang van herkennen en differentiaaldiagnose
Het is van belang om clozapinegeïnduceerde myoklonieën te herkennen zodat behandeling kan worden gestart en het risico op TC’s kan worden verlaagd. In de vier besproken studies kreeg 2,5-14% van de patiënten een TC.12-15 In een deel van deze gevallen zijn de epileptische myoklonieën een voorbode geweest.
Het symptoom myoclonus heeft een zeer uitgebreide etiologische differentiaaldiagnose (zoals stapelingsziekte, degeneratieve aandoeningen, (post)infectieuze oorzaken, metabole oorzaken, malabsorptiesyndromen, focale neurogene schade en epilepsiesyndromen) die we niet voldoende beknopt in deze casusbeschrijving kunnen samenvatten; hiervoor verwijzen we naar een overzichtsartikel.11 Wat betreft onze casus en het voorkomen van myoklonieën bij psychiatrische patiënten willen we benadrukken dat wijziging van de psychiatrische medicatie een belangrijke oorzaak kan zijn van het ontstaan van myoklonieën. Zo kunnen er negatieve myoklonieën (schokkende beweging door niet kunnen behouden van zelfde mate van spiertonus) ontstaan bij verlaging van de clozapinedosering16 en lijkt er sprake van een synergetische werking van clozapine met lithium waardoor myoklonieën vaker voorkomen bij tegelijktijdig gebruik.17
Daarnaast is het belangrijk om de epileptische (corticale) myoklonieën differentiaaldiagnostisch te kunnen onderscheiden van andere clozapinegeïnduceerde bewegingsstoornissen omdat de behandeling verschillend is.1,19 Bewegingen die op myoklonieën kunnen lijken, zijn:
– atone epileptische aanvallen en kataplexie (waarbij de spiertonus juist kortdurend wegvalt);
– vloeiende onwillekeurige doelloze bewegingen, zoals gezien worden bij (tardieve) dyskinesie;
– door de knieën knikken of zakken zoals bij clozapinegeïnduceerde hypotensie.
Deze differentiaaldiagnostische overwegingen vormen een basis voor het maken van een klinisch onderscheid en klinische (behandel)overwegingen. Bij vermoeden van epileptische aanvallen of bij onvoldoende verklaarde neurologische bewegingsstoornissen adviseren wij om de patiënt naar een neuroloog door te verwijzen.
Dosisrelatie
Een systematische review over de periode 1991-2009 toont een duidelijke relatie tussen plasmaspiegels van clozapine en het voorkomen van eeg-afwijkingen (gedefinieerd als focale of gegeneraliseerde trage activiteit, focale of gegeneraliseerde scherpe golven, pieken, piekgolven of polypieken).19 Voor een correlatie tussen plasmaspiegels van clozapine en het vóórkomen van epileptische aanvallen zijn wel aanwijzingen maar is er onvoldoende significant bewijs.19 Epileptische aanvallen komen vaker voor bij de opbouwfase van clozapine, derhalve is langzaam titreren geadviseerd.10,20
Behandeling
De behandeling van clozapinegeïnduceerde myoklonieën is niet gerandomiseerd onderzocht en derhalve gebaseerd op de mening van experts. Indien de dosis van clozapine niet kan worden verlaagd of het gebruik ervan gestaakt, heeft het de voorkeur patiënt door te verwijzen naar een neuroloog voor eventuele aanvullende diagnostiek en medicamenteuze behandeling. Bij clozapinegeïnduceerde epileptische myoklonieën is valproïnezuur de eerste behandelkeuze13,14,20 Dit heeft naast een anti-aanvalseffect ook een effect als stemmingsstabilisator.22 Wees echter terughoudend bij vrouwen in de vruchtbare levensfase vanwege (onder andere) de teratogeniciteit.23 Bij patiënten met nog onvoldoende behandelde psychotische stoornissen wordt lamotrigine geadviseerd, hoewel hierbij een risico bestaat op toename van de myoklonieën.20,24,25 Alternatieve behandelingen zijn topiramaat of gabapentine.20 Topiramaat kan hierbij ondersteunend zijn in de antipsychotische behandeling.4
Bij onze casus heeft de behandelend neuroloog ervoor gekozen om met topiramaat te starten op basis van literatuur gebaseerd op de mening van experts en het niet willen riskeren van meer (invaliderende) myoklonieën door lamotrigine. Carbamazepine wordt afgeraden in verband met een verhoogd risico op neutropenie in een behandelcombinatie met clozapine en vermindering van de effectiviteit van clozapine.26,27
Conclusie
Epileptische myoklonieën kunnen een bijwerking zijn van clozapine. De corticale oorsprong van de myoclonus kan worden vastgesteld met een eeg. Er is een significante positieve relatie tussen eeg-afwijkingen en de clozapinedosis. Behandeling bestaat bij voorkeur uit dosisverlaging of stoppen van de clozapine. Indien dit niet mogelijk is, wordt geadviseerd patiënt door te verwijzen naar de neuroloog. Bij bevestiging van de diagnose, is valproïnezuur de behandeling van eerste keuze (met uitzondering van vrouwen in de vruchtbare leeftijd). Epileptische myoklonieën dienen behandeld te worden omdat ze hinderlijk kunnen zijn voor de patiënt en waarschijnlijk ook een verhoogd risico geven op het krijgen van TC’s. Het is opvallend dat deze relatief vaak voorkomende bijwerking niet beschreven staat in het Farmacotherapeutisch kompas of bij het bijwerkingencentrum Lareb. Er is naar aanleiding van onze casus een melding gedaan bij Lareb over deze bevinding.
Literatuur
1 Farmacotherapeutisch kompas. www.farmacotherapeutischkompas.nl.
2 Hummer M, Kemmler G, Kurz M, e.a. Weight gain induced by clozapine. Eur Neuropsychopharmacol 1995; 5: 437-40.
3 Umbricht DSG, Pollack S, Kane JM. Clozapine and weight gain. J Clin Psychiatry 1994; 55: 157-60.
4 Clozapine Plus Werkgroep. Richtlijn voor het gebruik van clozapine. www.clozapinepluswerkgroep.nl/publicaties/richtlijn-voor-het-gebruik-van-clozapine.
5 Huisman R, Okhuijsen-Pfeifer C, Mulder EYH, e.a. Glasgow Antipsychotica Bijwerkingen Schaal voor Clozapine; validatie van de Nederlandstalige versie. Tijdschr Psychiatr 2021; 63: 270-5.
6 Antelo RE, Stanilla JK, Martin-Llonch N. Myoclonic seizures and ‘leg folding’ phenomena with clozapine therapy: Report of two cases. Biol Psychiatry 1994; 36: 759-62.
7 Berman I, Zalma A, DuRand CJ, e.a. Clozapine-induced myoclonic jerks and drop attacks. J Clin Psychiatry 1992; 53: 329-30.
8 Haddad PM, Sharma SG. Adverse effects of atypical antipsychotics: Differential risk and clinical implications. CNS Drugs 2007; 21: 911-36.
9 Haberfellner EM. Myoclonic and generalized tonic clonic seizures during combined treatment with low doses of clozapine and haloperidol. Eur Psychiatry 2002; 17: 55-6.
10 Devinsky O, Honigfeld G, Patin J. Clozapine-related seizures. Neurology 1991; 41: 369-71.
11 van der Salm SMA, Tijssen MAJ. Myoclonus. Een overzicht van symptoom tot therapie. Tijdschr Neurol Neurochir 2009; 110: 170-8.
12 Welch J, Manschreck T, Redmond D. Clozapine-induced seizures and EEG changes. J Neuropsychiatry Clin Neurosci 1994; 6: 250-6.
13 Malow BA, Reese KB, Sato S, e.a. Spectrum of EEG abnormalities during clozapine treatment. Electroencephalogr Clin Neurophysiol 1994; 91: 205-11.
14 Kikuchi YS, Sato W, Ataka K, e.a. Clozapine-induced seizures, electroencephalography abnormalities, and clinical responses in Japanese patients with schizophrenia. Neuropsychiatr Dis Treat 2014; 10: 1973-8.
15 Kitagawa K, Uekusa S, Matsuo K, e.a. Risk factors for clozapine-induced central nervous system abnormalities in Japanese patients with treatment-resistant schizophrenia. Asian J Psychiatr 2021; 60: 102652.
16 Kohlrausch FB, Severino-Gama C, Lobato MI, e.a. The CYP1A2 -163C>A polymorphism is associated with clozapine-induced generalized tonic-clonic seizures in Brazilian schizophrenia patients. Psychiatry Res 2013; 209: 242-5.
17 Rodin I, Evans A. Case of clozapine-associated negative myoclonus. J Clin Psychopharmacol 2023; 43: 386-7.
18 Elmarasi O, Abdelhady S, Pathare A, e.a. Clozapine- and lithium-associated myoclonus. J Clin Psychopharmacol 2024; 44: 57-58.
19 Osborne IJ, McIvor RJ. Clozapine-induced myoclonus: A case report and review of the literature. Ther Adv Psychopharmacol 2015; 5: 351-6.
20 Varma S, Bishara D, Besag FMC, e.a. Clozapine-related EEG changes and seizures: Dose and plasma-level relationships. Ther Adv Psychopharmacol 2011; 1: 47-66.
21 Treves IA, Neufeld MY. EEG abnormalities in clozapine-treated schizophrenic patients. Eur Neuropsychopharmacol 1996; 6: 93-4.
22 Kando JC, Tohen M, Castillo J, e.a. Concurrent use of clozapine and valproate in affective and psychotic disorders. J Clin Psychiatry 1994; 55: 255-7.
23 Tomson T, Marson A, Boon P, e.a. Valproate in the treatment of epilepsy in girls and women of childbearing potential. Epilepsia 2015; 56: 1006-19.
24 Muzyk A, Gala G, Kahn DA. Use of lamotrigine in a patient with a clozapine-related seizure. J Psychiatr Pract 2010; 16: 125-8.
25 Tiihonen J, Wahlbeck K, Kiviniemi V. The efficacy of lamotrigine in clozapine-resistant schizophrenia: a systematic review and meta-analysis. Schizophr Res 2009; 109: 10-4.
26 Iqbal MM, Rahman A, Husain Z, e.a. Clozapine: A clinical review of adverse effects and management. Ann Clin Psychiatry 2003; 15: 33-48.
27 Jerling M, Lindstrm L, Bondesson U, e.a. Fluvoxamine inhibition and carbamazepine induction of the metabolism of clozapine: Evidence from a therapeutic drug monitoring service. Ther Drug Monit 1994; 16: 368-74.
Appendices
Bijlage 1Authors
Merel Koopmans, neuroloog, Stichting Epilepsie Instellingen Nederland (SEIN), Heemstede.
Anne Koopmans, psychiater, i-psy, Utrecht.
Eline van Beijeren, neuroloog, SEIN, Heemstede.
Fieke Cox, neuroloog, SEIN, Heemstede.
Correspondentie
Dr. Merel Koopmans (mkoopmans@sein.nl).
Geen strijdige belangen meegedeeld.
Het artikel werd voor publicatie geaccepteerd op 4-9-2024.
Citeren
Tijdschr Psychiatr. 2024;66(10):615-618
