Ruimte in regels: juridische kaders van onderzoek met bestaande patiëntgegevens
Achtergrond Een subgroep van patiënten met ernstige psychische aandoeningen (EPA) is ondervertegenwoordigd in wetenschappelijk onderzoek, o.a. door belemmeringen rondom het geven van geïnformeerde toestemming. Dit kan leiden tot responsbias en gebrek aan kennis over deze groep. Retrospectief onderzoek met bestaande patiëntgegevens is voor sommige patiëntengroepen de enige manier waarop we onze kennis kunnen vergroten.
Doel Het doen van aanbevelingen om de mogelijkheid van retrospectief onderzoek met bestaande patiëntgegevens te benutten, rekening houdend met geldende wet- en regelgeving.
Methode Na een overzicht van de relevante wet- en regelgeving worden aanbevelingen gedaan.
Resultaten Factoren die de mogelijkheden voor retrospectief onderzoek bepalen, zijn 1. of gewerkt wordt met direct herleidbare, gepseudonimiseerde of geanonimiseerde gegevens; 2. of er een groot risico is op responsbias bij het vragen van geïnformeerde toestemming; 3. of informatie binnen de behandelrelatie wordt verzameld. Afhankelijk van de situatie zijn er verschillende alternatieven voor een procedure met geïnformeerde toestemming.
Conclusie Kennis van de relevante regelgeving en samenwerking met specialisten op dit gebied maakt retrospectief onderzoek met bestaande gegevens bij de subgroep van patiënten met EPA die geen geïnformeerde toestemming kunnen geven vaak mogelijk.
Patiënten met ernstige psychische aandoeningen (EPA) zijn in wetenschappelijk onderzoek ondervertegenwoordigd.1 Dit geldt met name voor een specifieke subgroep van patiënten, met behandelresistente symptomen, vaak meerdere diagnoses en complexe problemen, regelmatig zorgmijdend of met verplichte zorg, en vaak met een ander verklaringsmodel voor hun lijden dan de behandelaars.2 In Angelsaksische landen wordt deze groep wel omschreven als patiënten met ‘complex psychosis’ of ‘severe and persistent mental illness’ (SPMI).3-4 Een van de redenen van de ondervertegenwoordiging in wetenschappelijk onderzoek is dat er bij deze groep belemmeringen kunnen bestaan voor het geven van geïnformeerde toestemming (‘informed consent’) voor het meedoen aan wetenschappelijk onderzoek. Die belemmeringen komen bijvoorbeeld voort uit psychotische symptomen, met name paranoïdie, en cognitieve symptomen.
Bij onderzoek waarvoor geïnformeerde toestemming nodig is, kan het dus voorkomen dat de ernstigst aangedane patiënten relatief vaker geen toestemming geven. Dit kan de validiteit en generaliseerbaarheid van de resultaten verminderen; er is dan sprake van responsbias (een vorm van selectiebias).
Onderzoek naar verbetering van behandelmogelijkheden voor de groep met de ernstigste aandoening blijft hierdoor beperkt. Door gebrek aan valide beschrijvingen van problemen en prevalentie blijft deze groep bovendien nu relatief onzichtbaar in debatten over organisatie en financiering van zorg. Dit is relevant omdat het een groep betreft die ondanks de beperkte omvang een aanzienlijke impact heeft op het (zorg)systeem.5
Een van de mogelijkheden om toch onderzoek te doen bij deze groep is retrospectief wetenschappelijk onderzoek met bestaande patiëntgegevens (dossieronderzoek). Voor bepaalde patiëntengroepen kan dit de enige manier zijn waarop we onze kennis over het beloop en over mogelijke interventies kunnen vergroten. In dit essay behandelen we de juridische kaders van dit type onderzoek. Eerder gingen wij uitgebreid in op ethische afwegingen bij de ondervertegenwoordiging van bepaalde patiëntengroepen in wetenschappelijk onderzoek;2 de ethische kant stippen we in dit essay slechts zijdelings aan.
We doen aanbevelingen om de mogelijkheid van wetenschappelijk onderzoek met bestaande patiëntgegevens te benutten, rekening houdend met geldende wet- en regelgeving. Om onze aanbevelingen te onderbouwen gaan we in op de volgende vragen:
– Wat zijn in Nederland de juridische kaders bij dit type onderzoek?
– Welke eisen zijn er aan de procedure van geïnformeerde toestemming bij dit type onderzoek?
– Onder welke voorwaarden mag dit type onderzoek vanuit juridisch perspectief worden uitgevoerd zonder geïnformeerde toestemming?
– Welke mogelijkheden biedt dit voor onderzoek onder de subgroep van zeer ernstig aangedane patiënten met EPA?
Nederlandse juridische kaders voor onderzoek met bestaande patiëntgegevens
Wetenschappelijk onderzoek met bestaande patiëntgegevens valt niet onder de Wet medisch-wetenschappelijk-onderzoek met mensen (hierna: WMO) omdat de patiënten niet aan handelingen worden onderworpen en hun geen gedragsregels worden opgelegd.6 Wél van toepassing zijn de Wet op de geneeskundige behandelingsovereenkomst (Burgerlijk Wetboek boek 7, titel 7, afdeling 5, hierna: WGBO), de Algemene Verordening Gegevensbescherming (hierna: AVG) en de Uitvoeringswet AVG (hierna: UAVG). Daarnaast geldt er een gedragscode voor gezondheidsonderzoek: de Gedragscode Gezondheidsonderzoek van de Commissie Regelgeving Onderzoek (COREON). Dit is een gedragscode die gaat over het verantwoord omgaan met (persoons)gegevens en lichaamsmateriaal bij gezondheidsonderzoek.7 In het navolgende lichten we de relevante bepalingen nader toe.
WGBO
De WGBO bepaalt dat uitsluitend rechtstreeks betrokkenen (en hun vervanger) zonder voorafgaande toestemming kennis mogen nemen van patiëntgegevens, en alleen van díe gegevens die noodzakelijk zijn om hun rol te kunnen uitoefenen (het ‘medisch beroepsgeheim’).8 De hoofdregel voor het verrichten van wetenschappelijk onderzoek met gebruik van patiëntgegevens is dat daarvoor geïnformeerde toestemming van de patiënt nodig is.9
In de WGBO volgt het toestemmingsvereiste uit het medisch beroepsgeheim en uit de voorwaarden waaronder gegevens over een patiënt verstrekt mogen worden aan een derde. Als de arts zelf de onderzoeker is, hoeven geen patiëntgegevens verstrekt te worden aan een derde en geldt dit toestemmingsvereiste in juridische termen dus niet.10,11 Dit is alleen van toepassing als de behandelaar-onderzoeker een persoonlijke behandelrelatie heeft met de patiënt, en geldt niet voor een heel behandelteam.11
Geïnformeerde toestemming bij retrospectief onderzoek met bestaande gegevens
De patiënt kan alleen geïnformeerde toestemming geven als hij/zij wilsbekwaam is wat betreft de beslissing tot deelname aan dit specifieke onderzoek.
Voor zover ons bekend is er geen specifieke regelgeving voor niet-WMO-plichtig wetenschappelijk onderzoek met personen die wilsonbekwaam zijn wat betreft het geven van toestemming voor deelname. Dergelijke regelgeving is er wel voor WMO-plichtig onderzoek: het is in principe verboden, met uitzonderingen voor onderzoek dat de proefpersoon zelf ten goede kan komen (therapeutisch onderzoek) en onderzoek dat alleen met deze groep uitgevoerd kan worden én waarvan de risico’s en belasting minimaal zijn.12 In die gevallen mag de wettelijk vertegenwoordiger toestemming geven.13 Aangezien retrospectief dossieronderzoek gezien kan worden als een minder belastende variant van die laatste categorie, gaan wij ervan uit dat vervangende toestemming hierbij ook mogelijk is.
Uitzonderingsgronden voor het vragen van geïnformeerde toestemming
Het doen van niet-WMO-plichtig onderzoek door onderzoekers die geen behandelrelatie hebben met de patiënt is op grond van de WGBO zonder toestemming van de patiënt alleen mogelijk indien:14
1. Het vragen van toestemming in redelijkheid niet mogelijk is (bijvoorbeeld bij overleden patiënten) en er voorzien is in zodanige waarborgen, dat de persoonlijke levenssfeer van de patiënt niet onevenredig wordt geschaad, of
2. het vragen van toestemming in redelijkheid niet kan worden verlangd (bijvoorbeeld bij zeer grote aantallen patiënten, of aanmerkelijke kans op responsbias bij het vragen van toestemming) en de hulpverlener zorg heeft gedragen dat de gegevens in zodanige vorm worden verstrekt dat herleiding tot het individu redelijkerwijs wordt voorkomen (dus in gecodeerde/gepseudonimiseerde vorm).
3. Het onderzoek een algemeen belang dient.
4. Het onderzoek niet zonder de desbetreffende gegevens kan worden uitgevoerd; er is bijvoorbeeld geen mogelijkheid om met anonieme gegevens te werken.
5. De patiënt niet uitdrukkelijk bezwaar heeft gemaakt tegen gebruik van gegevens voor wetenschappelijk onderzoek.
Zoals we al beschreven, is er bij het vragen van geïnformeerde toestemming aan patiënten met een ernstige psychische aandoening een aanmerkelijke kans dat de ernstigst aangedane groep niet mee kan of wil doen op basis van bijvoorbeeld paranoïdie of cognitieve symptomen. Het is afhankelijk van de vraagstelling van de studie of hierdoor de resultaten worden beïnvloed. Als het doel is om ook of juist het profiel of beloop bij de ernstigst aangedane subgroep in beeld te brengen, is deze selectieve inclusie een wezenlijk probleem. Er is dan dus sprake van de uitzonderingsgrond ‘aanmerkelijke kans op responsbias bij het vragen van toestemming’. Aan de voorwaarden 3 en 4 kan met een goede onderzoeksopzet ook worden voldaan. De ‘geenbezwaarprocedure’ behorend bij voorwaarde 5 houdt in dat een patiënt geen toestemming hoeft te geven voor gebruik van zijn of haar gegevens voor onderzoek, maar dat hij of zij wel in de gelegenheid wordt gesteld om bezwaar te maken. Op deze geenbezwaarprocedure komen we verderop terug.
AVG en UAVG
Relevante overwegingen uit de AVG en UAVG om rekening mee te houden bij het doen van wetenschappelijk onderzoek zijn de volgende.
Voor de AVG geldt dat er een grondslag aanwezig moet zijn om persoonsgegevens (ook gecodeerde gegevens) te mogen verwerken voor een bepaald doel. Toestemming is een van de grondslagen volgend uit de AVG waarop de verwerking van gegevens binnen studieverband kan worden gebaseerd. De toestemming moet wel ‘vrijelijk’ worden gegeven, een actieve handeling betreffen vanuit betrokkene en kan op ieder moment ingetrokken worden (net zo gemakkelijk als dat de toestemming wordt verleend).15
De AVG voegt zich in dezen naar de bepalingen die volgen uit de WGBO (zie onder kopje WGBO) over het verrichten van wetenschappelijk onderzoek.16 Vanuit de AVG gelden aanvullende bepalingen gebaseerd op principes van doelbinding, noodzakelijkheid, subsidiariteit, passende technische en organisatorische maatregelen (waaronder pseudonimisering van gegevens en beveiligde gegevensopslag volgens de geldende normen).17
Anonimiseren en pseudonimiseren (coderen)
Juridische kaders zijn verschillend voor anonieme, gecodeerde en direct identificeerbare patiëntgegevens.
Volledig geanonimiseerde gegevens zijn geen persoonsgegevens meer omdat een natuurlijke persoon op geen enkele wijze meer direct of indirect identificeerbaar is op basis van die gegevens. Anonieme gegevens vallen daarom niet onder de AVG. Er wordt gesproken van geanonimiseerde gegevens als her-identificatie, gegeven de omstandigheden waaronder de data worden verwerkt én de huidige technische en statistische mogelijkheden, redelijkerwijs niet mogelijk is. Om te bepalen of in een specifieke situatie sprake is van anonieme gegevens is statistische, juridische en technische expertise vereist.7,18 Bij gezondheidsonderzoek ligt de lat erg hoog wil men van anonieme gegevens mogen spreken.
Gecodeerde gegevens, waarbij naam en geboortedatum zijn vervangen door een code, maar waarvan nog wel een sleutelbestand bestaat (ook als dat beheerd wordt door een derde partij), zijn géén geanonimiseerde gegevens. Dit worden ook wel gepseudonimiseerde gegevens genoemd.
Direct identificeerbare patiëntgegevens zijn gegevens met naam en geboortedatum. Iedere vorm van dossierinzage voor wetenschappelijk onderzoek houdt dus werken met direct identificeerbare patiëntgegevens in.
Praktische uitwerking van de regelgeving
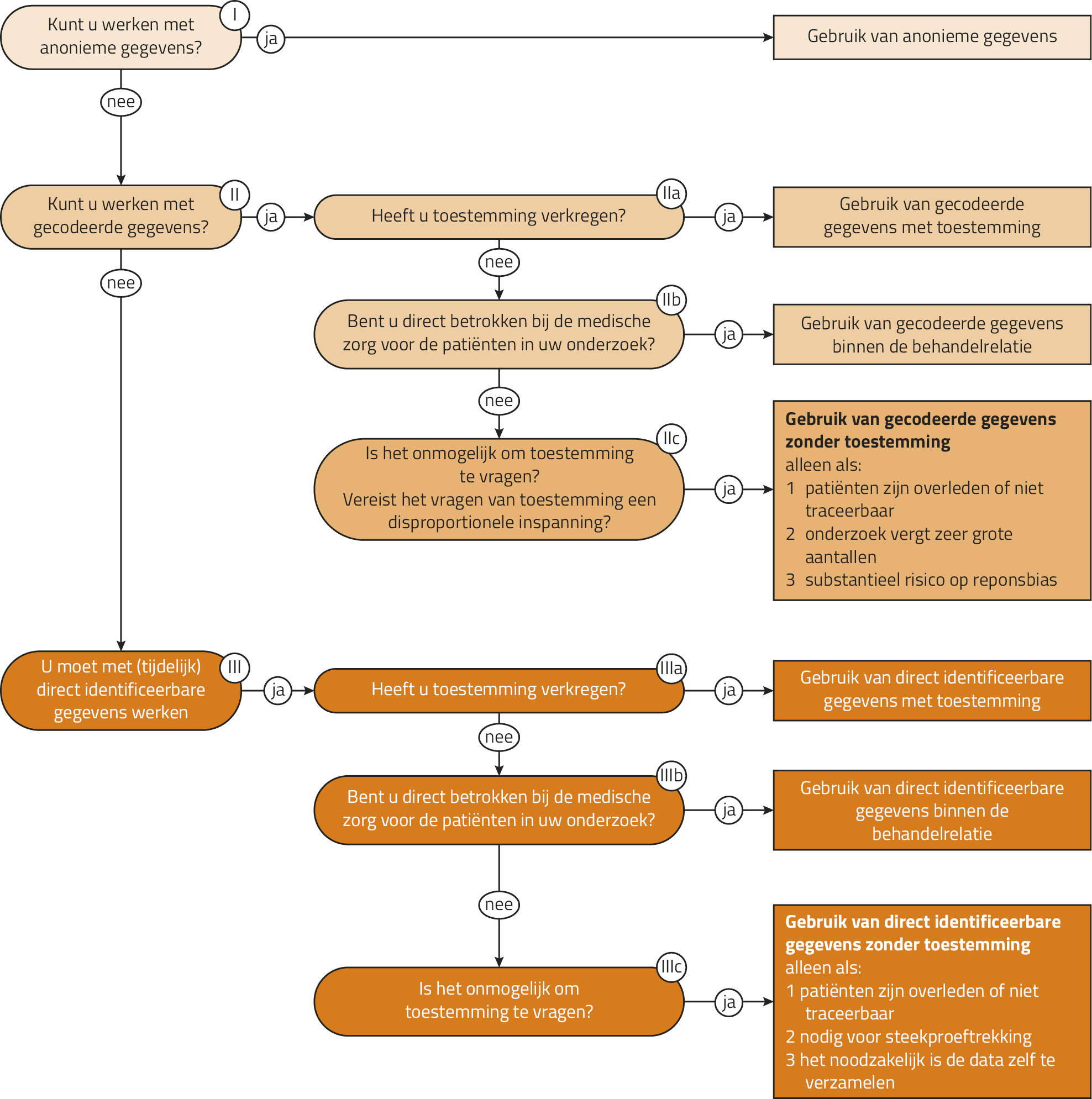
De omgang met de WGBO, AVG en UAVG bij het doen van onderzoek met bestaande patiëntgegevens, zoals in het voorgaande beschreven, is overzichtelijk weergegeven in een handreiking van Van Bon-Martens en Van Veen, ontwikkeld door een consortium van onder andere RIVM, Trimbos-instituut en GGD’en.10 Daarnaast hebben Scholte e.a. gedetailleerd beschreven hoe deze regels worden gehanteerd in het Amsterdam UMC.11 Inhoudelijk komen beide documenten op hoofdlijnen overeen. Beide bevatten een beslisboom (figuur 1 en 2). De beslisboom van Scholte e.a. (zie figuur 1) begint met de vraag of er gewerkt wordt met anonieme, gecodeerde of direct identificeerbare gegevens.11 Bij de beslisboom van Van Bon-Martens en Van Veen (zie figuur 2) is de vraag of de onderzoeker rechtstreeks betrokken is het startpunt.10 Omdat de startvraag van Scholte e.a. in onze ervaring beter aansluit op de wetenschappelijke praktijk, hanteren we deze indeling als uitgangspunt.
Figuur 1. Stroomdiagram volgens Scholte e.a. voor hergebruik van gegevens uit zorgdossiers voor wetenschappelijk onderzoek11
Figuur 2. Stroomdiagram volgens Van Bon-Martens en Van Veen ontsluiten bestaande patiëntgegevens voor wetenschappelijk onderzoek onder WGBO en AVG10
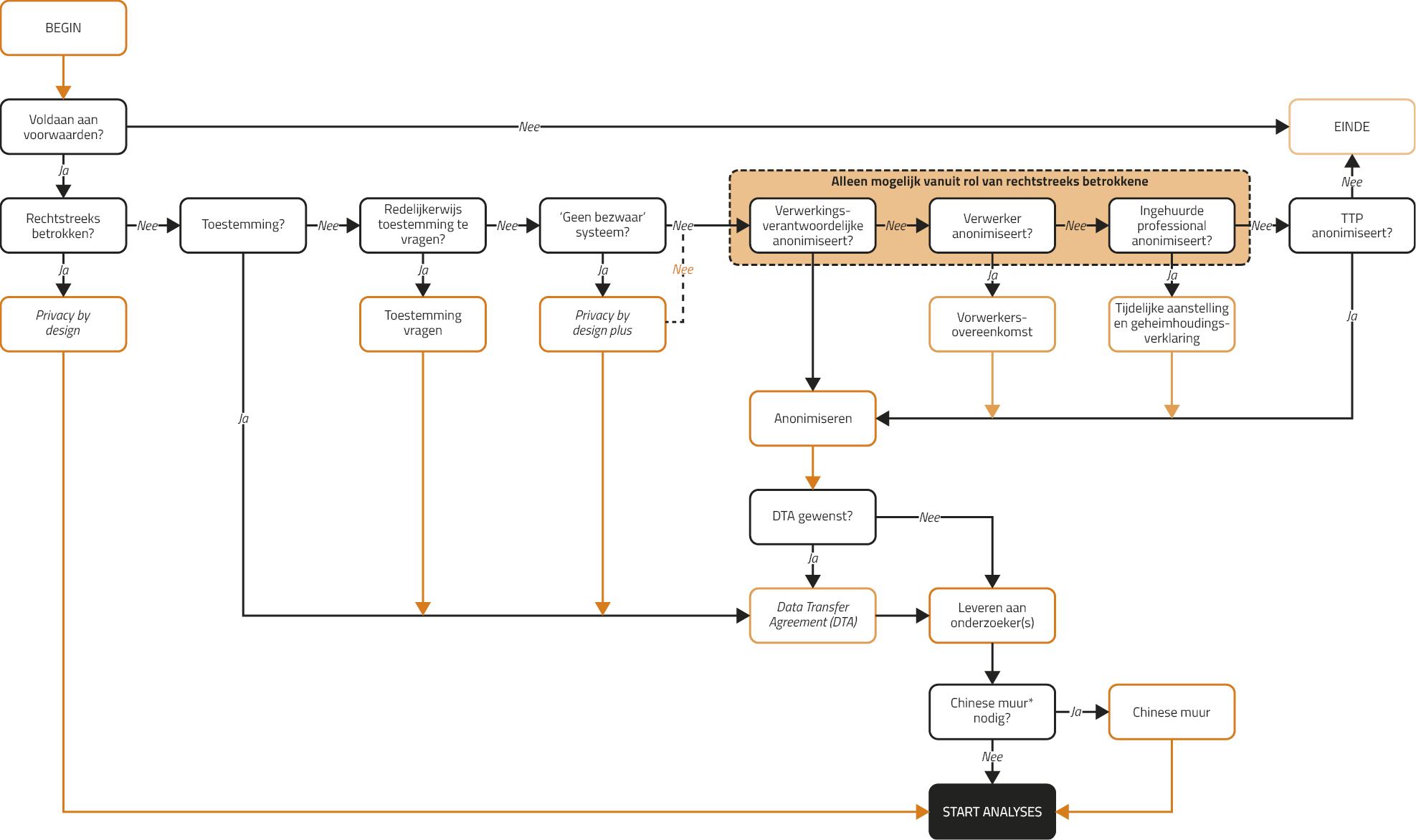
*Chinese muur: strikte scheiding tussen verschillende afdelingen, bijv. tussen degene die de persoonsgegevens heeft geanonimiseerd en de onderzoeker die deze anonieme gegevens gebruikt, om te voorkomen dat de onderzoeker de gegevens tot personen kan herleiden.
Het stroomdiagram van Scholte e.a. overziend (figuur 1), zien wij de volgende opties tot retrospectief onderzoek met bestaande patiëntgegevens bij de ernstigst aangedane groep patiënten met ernstige psychische aandoeningen, in studies waarbij toestemming vragen een groot risico op responsbias geeft:
Ten eerste: een studieopzet waarbij de gegevens worden verzameld door actuele behandelaren. Dit is dus alleen mogelijk als patiënten nog in behandeling zijn. Als behandelaar met een actuele behandelrelatie is het toegestaan om patiëntgegevens te gebruiken voor wetenschappelijk onderzoek, als het verkrijgen van geïnformeerde toestemming niet mogelijk of haalbaar is (opties IIb en IIIb in figuur 1). De behandelaar mag de gegevens verwerken. Als hij of zij de gegevens ter beschikking wil stellen aan andere onderzoekers, dan mag dit alleen in gecodeerde vorm. Dan gelden vervolgens de eisen die worden gesteld aan het werken met gecodeerde gegevens (zie optie 2).
Ten tweede: een studieopzet met bestaande, al gecodeerde gegevens. Als met gecodeerde gegevens gewerkt kan worden, dan volstaat een algemene geenbezwaarprocedure mits aan alle overige voorwaarden is voldaan (optie IIc-3 uit figuur 1). Hiervoor is het dus van belang dat een ziekenhuis of instelling een adequaat geïmplementeerde geenbezwaarprocedure heeft. Een belangrijke vraag is welke mogelijkheden er in praktijk zijn om met gecodeerde gegevens te werken. Bepaalde gegevens kunnen makkelijk gecodeerd aangeleverd worden uit het patiëntendossier aan onderzoekers door ICT-afdelingen omdat deze in specifieke velden in het elektronisch patiëntendossier worden ingevuld. Dit betreft bijvoorbeeld ROM-data, DSM-classificaties, toepassing van verplichte zorg, en behandelduur. Veel informatie over behandelgeschiedenis, effect en bijwerkingen van behandelingen, weigeringen van behandelingen, et cetera is echter ongestructureerd vastgelegd in brieven of beloopsnotities. Het is met datawetenschap toenemend mogelijk om ook deze gegevens geautomatiseerd uit dossiers te halen en middels algoritmen herleidbare informatie te verwijderen, zonder tussenkomst van personen/onderzoekers.
Ten derde: een studieopzet waarbij de benodigde data door onderzoekers zélf uit dossiers worden gehaald (optie IIIc-3 uit figuur 1): dit is alleen onder strenge voorwaarden toegestaan. Hier constateren we verschillen tussen Scholte e.a. versus Van Bon-Martens en Van Veen e.a.
Scholte e.a. werken de voorwaarden als volgt uit: er moet geen andere mogelijkheid zijn dan dat de onderzoeker de data zelf verzamelt, ieder patiëntendossier mag slechts eenmalig worden ingezien, de gegevens moeten meteen worden gecodeerd, de gegevensverzameling moet binnen een half jaar plaatsvinden, het sleutelbestand moet binnen een half jaar worden overgedragen, en het onderzoek moet getoetst zijn door een ethische commissie. Daarnaast vereisen Scholte e.a. een specifieke geenbezwaarbrief over de uit te voeren studie, met daarin het doel van het onderzoek, de te gebruiken gegevens, de betrokken personen en de bewaarduur, waarbij de patiënt laagdrempelig bezwaar kan maken. In de ‘Standard Operating Procedures Research Data Management’ van het Amsterdam UMC staat echter beschreven dat een substantieel, onderbouwd risico op responsbias reden kan zijn om van deze specifieke geenbezwaarbrief af te zien, in overleg met de medisch-ethische toetsingscommissie of niet-WMO-commissie en de functionaris gegevensbescherming. Er moet dan wél een algemene geenbezwaarprocedure geïmplementeerd zijn, bijvoorbeeld op de website van het ziekenhuis/de instelling.
Van Bon-Martens en Van Veen staan niet toe dat een onderzoeker zelf de data uit de dossiers verzamelt, tenzij deze onder directe verantwoordelijkheid van een rechtstreeks betrokken behandelaar werkt, met een geheimhoudingsverklaring (en dus afgeleid beroepsgeheim heeft). Dat kan dus alleen met patiënten die actueel in zorg zijn. In hun stroomschema mag dit ook als er géén algemene geenbezwaarprocedure is geïmplementeerd (want het beroepsgeheim wordt niet doorbroken), maar de voorwaarde is dan dat de gegevens geanonimiseerd worden (en niet gepseudonimiseerd/gecodeerd) vóór verdere verwerking door andere onderzoekers.
Ten vierde: een studieopzet waar bij wilsonbekwame deelnemers vervangende toestemming wordt gevraagd aan de wettelijk vertegenwoordiger. Zoals in het voorgaande beschreven, is dit juridisch toegestaan. In het stroomschema van Scholte e.a. kom je met vervangende toestemming in optie IIa of IIIa terecht, wat het onderzoek vergemakkelijkt.
Implementatie van geenbezwaarprocedures
Indien een ziekenhuis of instelling wetenschappelijk onderzoek met gecodeerde gegevens wil doen zonder voorafgaande toestemming, is een geïmplementeerde algemene geenbezwaarprocedure een verplichting. Dit kan via uitleg op de website en folders op afdelingen, in wachtkamers, en in informatiepakketten die patiënten en naasten krijgen uitgereikt. Hierin moet de uitleg staan dat gegevens verzameld in het kader van de reguliere zorg bij deze instelling ook gebruikt kunnen worden voor wetenschappelijk onderzoek, en de mogelijkheid om hiertegen bezwaar te maken moet duidelijk uitgelegd worden. Aangetekend bezwaar moet blijvend vindbaar zijn.
Landelijke samenwerkingen leerden ons dat veel algemene ziekenhuizen een dergelijke procedure hebben geïmplementeerd, maar veel ggz-instellingen niet. Om de mogelijkheden voor retrospectief onderzoek te vergroten is het wenselijk dat hier verandering in komt.
Zoals dat ook geldt voor verschillende subgroepen patiënten in algemene ziekenhuizen is het de vraag in hoeverre patiënten met ernstige psychische aandoeningen in staat zijn om deze informatie te begrijpen en ook werkelijk gebruik te maken van de bezwaaroptie. Daarom is het bij implementatie van belang dat folders/informatiepakketten ook worden uitgereikt aan naasten en/of wettelijk vertegenwoordigers, en dat behandelaren goede voorlichting krijgen over deze procedure, zodat zij deze zelf weer goed kunnen uitleggen.
Overwegingen
Onze ervaring is dat er in overleg tussen onderzoekers vaak verwarring ontstaat over de regelgeving. Wij hebben de indruk dat verschillende ziekenhuizen en instellingen, en verschillende functionarissen gegevensbescherming, hierin verschillende keuzes maken. Sommige medisch-ethische toetsingscommissies (METC’s) beoordelen ook bij niet-WMO-plichtig onderzoek kritisch of het voorstel voldoet aan de wet- en regelgeving, maar dat lijkt niet overal in dezelfde mate te gebeuren. Sommige instellingen hebben een eigen interne toetsingscommissie voor alle niet-WMO-plichtig onderzoek, of specifiek voor onderzoek met bestaande patiëntgegevens.
Wij zijn van mening dat deze praktijkvariatie leidt tot twee risico’s. Enerzijds bestaat het risico dat onderzoek met bestaande patiëntgegevens plaatsvindt zonder voldoende rechtsbescherming voor patiënten, waardoor rechtsongelijkheid kan ontstaan. Anderzijds is het risico dat de bestaande mogelijkheden onvoldoende benut worden, terwijl deze cruciaal zijn om voldoende kennis te vergaren over complexe en weinig onderzochte patiëntengroepen. Beide zijn niet in het belang van deze kwetsbare groep.
Aanbevelingen voor onderzoek met bestaande patiëntgegevens
– Implementeer een goede algemene geenbezwaarprocedure voor gebruik van bestaande patiëntgegevens voor wetenschappelijk onderzoek in iedere instelling. Stel een werkwijze op waarbij deze informatie ook terechtkomt bij naasten en/of wettelijk vertegenwoordigers.
– Hanteer het uitgangspunt dat geïnformeerde toestemming nodig is voor ieder onderzoek, óók voor onderzoek met bestaande patiëntgegevens. Als er een groot risico is op responsbias, doorloop dan een van de hier besproken stroomdiagrammen en overweeg de in het voorgaande besproken opties. Het verdient aanbeveling het risico op selectieve inclusie te testen in een pilotstudie alvorens te concluderen dat de beoogde studie niet met geïnformeerde toestemming kan worden uitgevoerd.
– Leg ieder voorstel voor onderzoek met bestaande patiëntgegevens voor aan een interne toetsingscommissie en/of aan de functionaris gegevensbescherming, om te toetsen of voldaan is aan alle vereisten vanuit WGBO en AVG.
– Leg ieder voorstel voor onderzoek met bestaande patiëntgegevens voor aan een erkende METC voor een niet-WMO-verklaring.
Conclusie
Voor het verbeteren van de behandeluitkomsten van de meest complexe patiëntengroepen, is wetenschappelijk onderzoek onmisbaar. De rechtsbescherming en rechtsgelijkheid van de kwetsbare patiënt, zeker bij wilsonbekwaamheid, is een groot goed. Voor de uitvoering van wetenschappelijk onderzoek met bestaande patiëntgegevens is het daarom van belang dat er voldoende kennis is onder onderzoekers van de regelgeving hieromtrent. Wet- en regelgeving bieden meer ruimte dan nu benut wordt, al zijn de uitwerkingen van deze ruimte niet altijd eenduidig. Zoek dus samenwerking met specialisten op dit gebied. Ons advies: houd je aan de regels, maar benut de ruimte die de regels bieden, in het belang van deze te vaak onzichtbare patiëntengroep.
Literatuur
1 Delespaul Ph en de consensusgroep EPA. Consensus over de definitie van mensen met een ernstige psychische aandoening (EPA) en hun aantal in Nederland. Tijdschr Psychiatr 2013; 55: 427-38.
2 De Koning MB, Burger TJ, Van Eck R, e.a. De ondervertegenwoordiging van complexe patiëntengroepen in wetenschappelijk onderzoek: ethische overwegingen. Tijdschr Psychiatr 2021; 63: 731-6.
3 NICE Guideline. Rehabilitation for adults with complex psychosis 2020; www.nice.org.uk/guidance/ng181.
4 Zumstein N, Riese F. Defining severe and persistent mental illness – a pragmatic utility concept analysis. Front Psychiatry 2020; 11: 648.
5 Killaspy H, Marston L, Green N, e.a. Clinical outcomes and costs for people with complex psychosis; a naturalistic prospective cohort study of mental health rehabilitation service users in England. BMC Psychiatry 2016; 16: 95.
6 Artikel 1 WMO.
7 Commissie Regelgeving Onderzoek (COREON). Gedragscode Gezondheidsonderzoek. 2022. https://www.coreon.org/wp-content/uploads/2022/01/Gedragscode-Gezondheidsonderzoek-2022.pdf
8 Artikel 7:457 BW.
9 Artikel 7:457 lid 1 jo. 7:458 BW.
10 Van Bon-Martens M, van Veen EB. Handreiking ontsluiten patiëntgegevens voor onderzoek: werken volgens de regels uit AVG, UAVG en WGBO. Juli 2019. www.rivm.nl/sites/default/files/2019-09/Handreiking%20ontsluiten%20patientgegevens.pdf
11 Scholte R, Kranendonk E, Paardekooper M, e.a. Hergebruik van patiëntgegevens voor wetenschappelijk onderzoek: op weg naar eenduidige spelregels. Tijdschrift voor Gezondheidswetenschappen 2019; 97: 55-8.
14 Artikel 7:458 BW.
15 Artikel 9 lid 2 sub j AVG, artikel 89 AVG en artikel 24 UAVG.
16 Artikel 24 UAVG.
17 Artikel 5 en 6 AVG.
18 Preambule paragraaf 26 AVG.
Auteurs
Mariken de Koning, psychiater, Mentrum (onderdeel van Arkin); plv. A-opleider; senior onderzoeker, Arkin en Amsterdam UMC, locatie AMC, Amsterdam.
Thijs Burger, psychiater, Mentrum (onderdeel van Arkin); promovendus, Arkin en Amsterdam UMC locatie AMC, Amsterdam.
Astrid Vellinga, psychiater, Mentrum (onderdeel van Arkin); plv. geneesheer-directeur; senior onderzoeker, Arkin, Amsterdam.
Robin Van Eck, psychiater, Invivo Clinics, Amstelveen; promovendus, Amsterdam UMC locatie AMC, Amsterdam.
Martijn Kikkert, psycholoog, senior onderzoeker en afdelingshoofd, afd. Onderzoek, Arkin, Amsterdam.
Lieuwe de Haan, psychiater en hoogleraar Psychotische stoornissen, Amsterdam UMC, locatie AMC; voorzitter Academische Werkplaats EPA Arkin, Amsterdam.
Hans de Haas, psychiater, Inforsa (onderdeel van Arkin); senior onderzoeker, Arkin en Amsterdam UMC locatie AMC, Amsterdam.
Correspondentie
Dr. Mariken de Koning (mariken.de.koning@mentrum.nl).
Geen strijdige belangen meegedeeld.
Het artikel werd voor publicatie geaccepteerd op 19-6-2024.
Citeren
Tijdschr Psychiatr. 2024;66(8):437-442
Noot
Mr. S. Horst, jurist en privacy officer bij Arkin, en G. Megens, functionaris gegevensbescherming, deden waardevolle suggesties voor dit artikel.
